Contente
Calor específico, calor sensível e calor latente são quantidades físicas:
o calor específico de uma substância é a quantidade de calor que deve ser fornecida a uma unidade de massa dessa substância para aumentar sua temperatura em uma unidade. Essa quantidade varia muito, dependendo da temperatura em que a substância está antes que o calor seja aplicado a ela. Por exemplo, é necessária uma caloria para aumentar em um grau a água à temperatura ambiente, mas leva apenas 0,5 caloria para aumentar a temperatura do gelo em -5 graus em um grau. O calor específico também depende da pressão atmosférica. A mesma substância em uma pressão atmosférica mais baixa tem um calor específico mais baixo. Os exemplos abaixo são válidos para uma temperatura de 25 graus e uma pressão de 1 atmosfera.
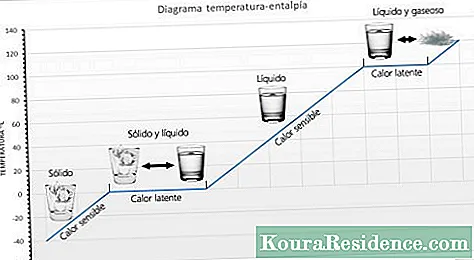
o calor sensível É a quantidade de calor que um corpo pode receber sem afetar sua estrutura molecular. Se a estrutura molecular não muda, o estado (sólido, líquido, gás) não muda. Como a estrutura molecular não muda, observa-se uma mudança na temperatura, razão pela qual é chamada de calor sensível.
o calor latente é a energia (calor) necessária para uma substância mudar de fase (estado). Se a mudança for de sólido para líquido, é chamada de calor de fusão. Se a mudança for de líquido para gasoso, é chamada de calor de vaporização. Quando o calor é aplicado a uma substância que atingiu a temperatura em que muda de estado, é impossível que a temperatura aumente, ela simplesmente muda de estado. Por exemplo, se o calor continuar a ser aplicado à água fervente, ele nunca excederá 100 ° C. Dependendo da substância, o calor latente geralmente pode ser medido em calorias por grama ou em quilojoules por quilograma (KJ).
Exemplos de calor específico
- Água (no estado líquido): 1 caloria por grama para aumentar 1 ° C
- Alumínio: 0,215 calorias por grama
- Berílio: 0,436 calorias por grama
- Cádmio: 0,055 calorias por grama
- Cobre. 0,0924 calorias por grama
- Glicerina: 0,58 calorias por grama
- Ouro: 0,0308 calorias por grama
- Ferro: 0,107 calorias por grama
- Chumbo: 0,0305 calorias por grama
- Silício: 0,168 calorias por grama
- Prata: 0,056 calorias por grama
- Potássio: 0,019 calorias por grama
- Tolueno: 0,380 calorias por grama
- Vidro: 0,2 calorias por grama
- Mármore: 0,21 calorias por grama
- Madeira: 0,41 calorias por grama
- Álcool etílico: 0,58 calorias por grama
- Mercúrio: 0,033 calorias por grama
- Azeite: 0,47 calorias por grama
- Areia: 0,2 calorias por grama
Exemplos de calor sensível
- Aplique calor à água que esteja entre 1 e 100 ° C
- Aplique calor à lata que seja inferior a 240 ° C
- Aplique calor de chumbo abaixo de 340 ° C
- Aplique calor ao zinco abaixo de 420 ° C
- Aplique calor ao alumínio inferior a 620 ° C
- Aplique calor ao bronze inferior a 880 ° C
- Aplique calor ao níquel abaixo de 1450 ° C
Exemplos de calor latente
Água: calor latente de fusão: 80 calorias por grama (leva 80 calorias para um grama de gelo a 0 ° C para se tornar água), calor latente de vaporização: 540 calorias por grama (leva 540 calorias para um grama de água a 100 ° C para se transformar em vapor).
Aço: calor latente de fusão: 50 calorias
Alumino: calor latente de fusão: 85 calorias / 322-394 KJ; calor latente de vaporização: 2300 KJ.
Enxofre: calor latente de fusão: 38 KJ; calor latente de vaporização: 326 KJ.
Cobalto: calor latente de fusão: 243 KJ
Cobre: calor latente de fusão: 43 calorias; calor latente de vaporização: 2360 KJ.
Estanho: calor latente de fusão: 14 calorias / 113 KJ
Fenol: calor latente de fusão: 109 KJ
Ferro: calor latente de fusão: 293 KJ; calor latente de vaporização: 2360 KJ.
Magnésio: calor latente de fusão: 72 calorias
Mercúrio: calor latente de fusão: 11,73 KJ; calor latente de vaporização: 356,7 KJ.
Níquel: calor latente de fusão: 58 calorias
Prata: calor latente de fusão: 109 KJ
Chumbo: calor latente de fusão: 6 calorias; calor latente de vaporização: 870 KJ.
Oxigênio: calor latente de fusão: 3,3 calorias
Ouro: calor latente de fusão: 67 KJ
Zinco: calor latente de fusão: 28 calorias


